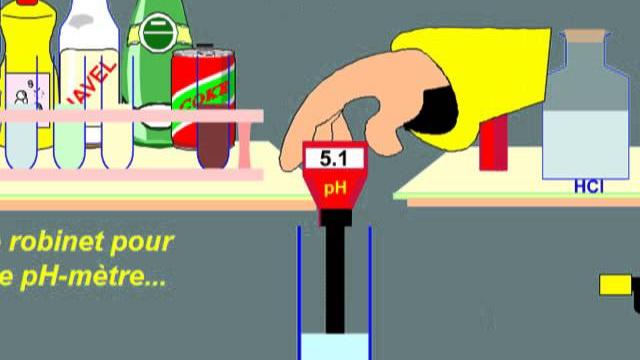
تسمى المواد التي تطلق أيونات الهيدروجين الموجبة في الماء ، لأن المواد تختلف عند وضعها في الماء أو في حلول مختلفة تطلق أيونات يمكن أن تكون أيونات موجبة أو سالبة ، ويمكن أن تتأين هذه المواد كليا أو جزئيا ، مما يؤدي إلى الطبيعة المختلفة للمادة ، وفي الأسطر التالية سنتحدث عن الإجابة على هذا السؤال.
تسمى المواد التي تطلق أيونات الهيدروجين الإيجابية في الماء
تسمى المواد التي تطلق أيونات الهيدروجين الإيجابية في الماء بالأحماض ، حيث تتميز الأحماض بحقيقة أنه عند وضعها في حلول مختلفة مثل الماء ، فإنها تطلق أيون موجب أو ما يسمى بروتون ، أيون هيدروجين إيجابي ، على عكس القواعد. أنه عند وضعها في حلول مختلفة مثل الماء ، فإنها تتأين وتعطي الأيونات السالبة ، أو ما يعرف بالإلكترونات ، هي أيونات هيدروكسيد ، لذلك عندما تتفاعل الأحماض مع القواعد ، يحدث التفاعل بسهولة ويتبعه تكوين الملح والماء. . لأن أحدهما يطلق بروتونا إيجابيا والآخر يطلق إلكترون سالب يسبب التفاعل بينهما وهو القاعدة التي تصنع عليها الأملاح بشكل مختلف حيث يحدث التفاعل بين الحمض والقاعدة لتشكيل الملح والماء.
أهم الخصائص التي تميز الأحماض.
هناك العديد من الخصائص والمزايا التي تميز الحمض عن المواد الكيميائية الأخرى المختلفة ، خاصة:
- تتميز الأحماض بإعطاء أيونات موجبة في الماء عند وضعها فيه أو محاليل أخرى ، وهذه الأيونات الموجبة هي أيونات الهيدروجين.
- تغيير ورقة عباد الشمس الحمضية من الأزرق إلى الأحمر ، على عكس القواعد التي تغير ورقة عباد الشمس من الأحمر إلى الأزرق.
- الأحماض لها طعم حامضي.
- الأحماض لها درجة الحموضة من صفر إلى سبعة.
- الأحماض تتفاعل مع القواعد لتشكيل الملح والماء ، مثل ملح الطعام أو كلوريد الصوديوم.
- من المعروف أن المحاليل الحمضية موصلات جيدة للكهرباء.
- الأحماض القوية غالبا ما تسبب حروق الجلد ، لذا كن حذرا.
- الأحماض المستخدمة في العديد من الاستخدامات في الحياة العملية ، حيث يتم استخدامها في الحفاظ على الغذاء وفي صناعة البطاريات والمتفجرات والأسمدة والمشروبات الغازية وغيرها.
الفرق بين حمض قوي وضعيف.
ليس كل الأحماض لها نفس القوة والقدرة على التأين ، ولكن هناك مجموعة من الأحماض التي تتأين تماما في حلول مختلفة وتعطي أيونات الهيدروجين ، وأهمها حمض الهيدروكلوريك وحمض الكبريتيك وحمض النيتريك ، إلخ.، والأحماض الضعيفة هي تلك التي لا تتأين تماما في الماء ، أو في حلول مختلفة ، أمثلة على هذه الأحماض هي حمض الخليك ، حمض الفوسفوريك ، وغيرها.
أخيرا ، لقد أجبنا على السؤال عن المواد التي تطلق أيونات الهيدروجين الإيجابية في الماء المسمى ؟ ، علمنا عن أهم الخصائص التي تميز الأحماض من المواد الأخرى ، فضلا عن أهم المعلومات والاختلافات بين الأحماض القوية والجيدة. وتسمى الأحماض الضعيفة ، وكذلك المواد التي تطلق أيونات الهيدروجين الإيجابية في الماء.
